PROPRIETA’ DEI VETRI : LA VISCOSITA’
E’ una proprietà dei vetri importante sia sotto l’aspetto scientifico che tecnologico: numerose sono le problematiche che si collegano alla viscosità, per rammentarne alcune si pensi al processo di refining, a quello di formatura, alla nucleazione ed accrescimento di fasi cristalline nei vetri, al fenomeno della immiscibilità.
La viscosità dipense fondamentalmente da tre parametri: la temperatura, la composizione chimica e la storia termica cioè il modo con cui il vetro si è formato dallo stato di fuso.
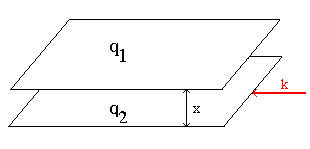
Si supponga di suddividere un fluido (il fuso ad esempio) in piani di superficie q separati da una distanza x (figura 1)
Figura 1

se applichiamo una forza tangenziale k tale che gli strati si muovano l’uno rispetto all’altro con velocità v, allora sarà valida la relazione
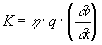
dove ![]() è il gradiente della velocità, la forza è di tipo newtoniano ed il fattore di proporzionalità h è detto viscosità. L’inverso della viscosità è detto fluidità
è il gradiente della velocità, la forza è di tipo newtoniano ed il fattore di proporzionalità h è detto viscosità. L’inverso della viscosità è detto fluidità ![]() .
.
Se i due piani hanno superficie di 1 m2 e distano 1 m, la viscosità assume il valore unitario in Pa.s quando la forza applicata è di 1 N. In genere la viscosità dei vetri viene espressa in Poise che equivalgono ad 1 dPa.s (un deci-pascal secondo).
1.1) Dipendenza viscosità-temperatura
La viscosità è un processo cinetico di attivazione e quindi la sua dipendenza dalla temperatura può essere descritta dalla relazione di Boltzmann:
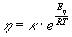
dove Eh è l’energia di attivazione dello scorrimento viscoso ed R è la costante dei gas. Questa relazione rappresenta solo una approssimazione del reale comportamento di un fluido viscoso, essa sarebbe infatti valida per fluidi ideali con particelle perfettamente sferiche e perfettamente isotropi dal punto di vista delle forze di legame.
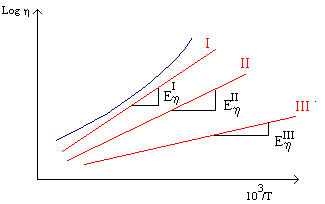
Se costruiamo il grafico del log h contro l’inverso della temperatura (figura 2) per diversi tipi di vetri si ottengono delle rette la cui pendenza rappresenta Eh .
I vetri con bassi valori di energia di attivazione dello scorrimento viscoso sono detti del III tipo o "dolci": la viscosità varia poco in un ampio intervallo di temperatura, questi vetri sono i più adatti a subire lavorazioni quali processi di formatura o laminazione.
I vetri con alti valori di energia di scorrimento viscoso sono detti del I tipo o "corti", in questo caso la viscosità varia notevolmente in un piccolo intervallo di temperatura, la lavorazione diventa più difficile perché richiede un accurato controllo della temperatura.
Spesso non si hanno relazioni lineari tra viscosità e temperatura (curva in blu) e questo è una ulteriore conferma dell’esistenza nel vetro di strutture complesse (clusters, aggregati molecolari ...) che si oppongono al progressivo allentamento del network all’aumentare della temperatura.(Vedi la teoria degli ioni discreti).
Fig.2
Il vetro di silice pura a causa della struttura del network con forti legami Si-O ha una Eh .di 711 103 J mol-1 mentre per vetri borosilicatici commerciali questo valore varia mediamente da 83 a 650 J mol-1
Fig.3
§ 5.5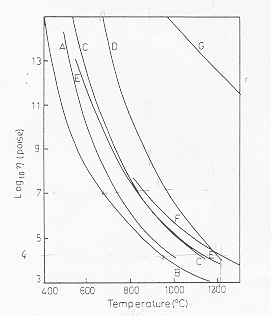
Dalla figura 3 § 5.5 vediamo la relazione viscosità-temperatura per alcuni vetri commerciali: vediamo che il vetro di tipo B per contenitori da vuoto è più dolce di quello di tipo D, quest’ultimo ha dunque un minore intervallo di lavorabilità.
Come si è accennato la relazione di Boltzmann non fornisce un accordo soddisfacente con i valori sperimentali: per questa ragione viene normalmente utilizzata una relazione empirica scoperta da Vogel Fulcher e Tammann e chiamata per questo equazione V-F-T (figura 4)§ 5.6.
Fig.4
§ 5.6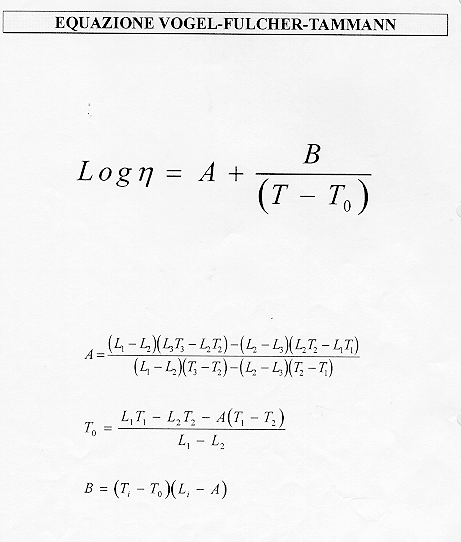
![]() equazione V.F.T.
equazione V.F.T.
Come vediamo dalla equazione vengono introdotte tre costanti A, B, T0 il cui calcolo, mostrato nella parte inferiore della figura, fa uso del valore della viscosità log h i ad una data temperatura.
Nella pratica il problema viene ulteriormente semplificato calcolando il valore della viscosità a tre specifiche temperature, ad esempio per un vetro commerciale per termometri abbiamo:
Tab.1
|
punto caratteristico |
log h |
Temperatura T |
|
temperatura di trasformazione Tg |
13,3 |
550 °C |
|
temperatura di Littleton ( softening point) |
7,6 |
715 °C |
|
working point |
4,0 |
1000 °C |
il sistema di equazioni diventa:
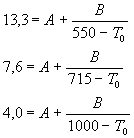
risolvendo il sistema si ottiene A = -1,386, B = 3830,3, T0 = 288,8 quindi l’equazione V-F-T sarà:
![]()
1.2) Metodi di misura
Nei vetri il range della viscosità è così ampio ( log h = 1-20) che non è possibile adottare un solo metodo di misura).
1.2.1) viscosimetro a caduta
Una sfera di platino di raggio r viene lasciata cadere in un crogiolo di raggio Rc riempito di vetro fuso, si misura il tempo impiegato a percorrere una distanza x, la viscosità è data da:
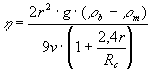
dove g è l’accelerazione di gravità, r b è la densità della sfera di platino, r m è la densità del fuso e v è la velocità di caduta della sfera. Nella equazione il termine che appare tra parentesi al denominatore è calcolato empiricamente e tiene conto della geometria del contenitore, il range di misura varia tra log h = 2 e log h = 7
1.2.2) viscosimetro a vibrazione
Questo metodo serve a misurare viscosità molto basse, si basa sullo smorzamento di un corpo appeso nel fuso ad un cavo di torsione; se il rapporto tra le ampiezze di due smorzamenti consecutivi è k e conseguentemente ![]() allora la viscosità sarà data da:
allora la viscosità sarà data da:
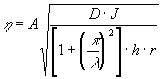
dove D è la forza direzionale agente sul cavo di torsione, J rappresenta il momento di inerzia del corpo vibrante ed A è una costante che tiene conto della geometria dello strumento. h ed r rappresentano rispettivamente la profondità di immersione dell’oggetto (in genere una sfera) ed il suo raggio. Il range di misura va da log h = 1 a log h = 4.
1.2.3) viscosimetro a rotazione
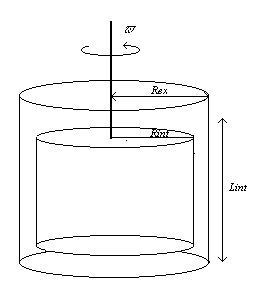
E’ il metodo più versatile e quindi più adottato per la misura della viscosità, con esso si copre un grande range di viscosità: ![]() , un elemento ruotante di platino che può essere cilindrico o sferico è immerso in un fuso a sua volta contenuto in un cilindro esterno ugualmente di platino, l’esperimento può essere condotto facendo ruotare il cilindro interno rispetto a quello esterno tenuto fisso oppure si possono far ruotare entrambi e quindi misurare la forza di torsione necessaria per mantenere una velocità relativa v.(figura 5).
, un elemento ruotante di platino che può essere cilindrico o sferico è immerso in un fuso a sua volta contenuto in un cilindro esterno ugualmente di platino, l’esperimento può essere condotto facendo ruotare il cilindro interno rispetto a quello esterno tenuto fisso oppure si possono far ruotare entrambi e quindi misurare la forza di torsione necessaria per mantenere una velocità relativa v.(figura 5).
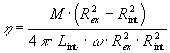
Dove Rex è il raggio del cilindro esterno, Rint è il raggio del cilindro interno, Lint è la profondità di immersione del cilindro interno nel fuso, w è la velocità di rotazione angolare ed M è la forza di torsione.
Fig. 5
1.2.4) viscosimetro ad elongazione
Viene utilizzato per la misura di alte viscosità ( log h = 6-14,5) come ad esempio il punto di Littleton nei vetri commerciali, un filamento di vetro di dimensioni standard viene posto in una muffola e sottoposto ad un dato gradiente termico ( in genere 0,1-1 ![]() ) se ad una sua estremità viene applicato un carico F la viscosità si ottiene con la seguente relazione:
) se ad una sua estremità viene applicato un carico F la viscosità si ottiene con la seguente relazione:
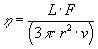
dove L è la lunghezza della fibra di vetro, F il carico applicato, r il raggio della fibra e v la velocità di allungamento.
1.2.5) viscosimetro a penetrazione
Una sfera od un cilindro con punta conica di platino di raggio R e sottoposto ad un carico F penetra nel vetro fuso: si misura la profondità di penetrazione l ed il tempo t impiegato:
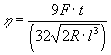
Con questo sistema si misurano valori del logaritmo della viscosità fino a 13
1.2.5) viscosimetro a flessione
Per valori di viscosità superiori a log h = 13 si misura l’entità della deformazione prodotta su una barretta di vetro sottoposta ad una data temperatura T ed un carico noto P.
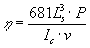
dove Ic è il momento di inerzia pari a ![]() per un campione di sezione rettangolare mentre il fattore numerico a numeratore include l’accelerazione di gravità (tutte le lunghezze in mm).
per un campione di sezione rettangolare mentre il fattore numerico a numeratore include l’accelerazione di gravità (tutte le lunghezze in mm).
Per misurare viscosità ancora più alte (log h da 12 a 16) si utilizza un metodo basato sulla torsione di un tubo di vetro cavo o pieno, conoscendo la forza di torsione T e misurando la velocità angolare w della torsione si ottiene:
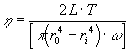
dove L è la lunghezza del tubo ed r0 ed ri sono il raggio esterno ed interno, se è utilizzato un tubo pieno allora nella formula ri = 0.
Nella pratica si preferisce misurare i valori della viscosità a temperature caratteristiche e con metodi standardizzati:
1) temperatura di trasformazione vetrosa: viene misurata con il dilatometro, si calcola dall’intersezione delle tangenti ai due rami della curva di dilatazione del vetro intorno alla Tg, in genere a questa temperatura il log h = 13, per misure più precise si utilizza uno dei metodi descritti sopra alla temperatura di transizione vetrosa trovata (in genere con il viscosimetro a rotazione).
2) punto di Littleton: si sospende un filamento di vetro di diametro pari a 0,65 ± 0,01 mm e di lunghezza 235 ± 0,1 mm in una muffola con un gradiente termico di 1°K/5min.in modo che la sua estremità inferiore sia libera: si raggiunge il punto di Littleton (o softening point) quando si registra un allungamento del filamento di 1 mm/minuto, in questo caso il log h = 7,6.
3) working point: si trova nelle vicinanze della temperatura di fusione, un cilindro con alla sommità una emisfera viene fatto sprofondare nel vetro tenuto ad una data temperatura, sfruttando la relazione: ![]() ed utilizzando un cilindro in lega Pt/Rh 90:10 di lunghezza di 50 mm con estremità arrotondate e di massa di 0,902 g si raggiungerà il working point (log h = 4) alla temperatura per la quale si raggiunge la profondità l di 20 mm in 60 secondi di tempo.
ed utilizzando un cilindro in lega Pt/Rh 90:10 di lunghezza di 50 mm con estremità arrotondate e di massa di 0,902 g si raggiungerà il working point (log h = 4) alla temperatura per la quale si raggiunge la profondità l di 20 mm in 60 secondi di tempo.
1.3) Dipendenza della viscosità dalla composizione
1.3.1) Sistemi monocomponenti
Fig. 6
§ 5.8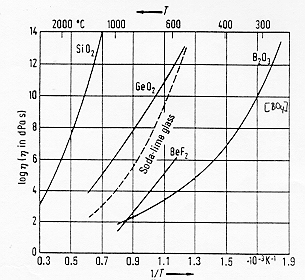
Come vediamo dalla figura 6 § 5.8 per un vetro di silice il logaritmo della viscosità cresce molto con l’inverso della temperatura, questo è dovuto al fatto che la struttura presenta forti legami Si-O i quali, all’aumentare della temperatura, subiscono rotture graduali come previsto dal modello teorico del network continuo. Il vetro è classificabile come "corto" mentre la relazione viscosità-temperatura è, come ci si poteva aspettare, praticamente lineare. Anche il sistema GeO2 in quanto costituito da un elemento formatore di vetro presenta una relazione lineare anche se, in questo caso i legami Ge-O sono più deboli di quelli Si-O. Nel caso del BeF2 si ha una struttura ancora più debole; l’elettronegatività dell’anione F- è tanto elevata che allo stato di fuso il sistema va verso un modello tipo "Frenkel". Il sistema B2O3 si discosta dai precedenti a causa della non linearità della correlazione viscosità-temperatura; la struttura è, come vediamo, assai più debole di quella del vetro di silice a causa della ibridazione sp2 (trigonale) del boro mentre la non linearità si può spiegare a temperature inferiori con la polarizzabilità del legame B-O e con la tendenza alla formazione di unità [BO4]. Anche la viscosità del sistema P2O5 può apparire sorprendentemente bassa ma questo si spiega con il fatto che l’unità strutturale [PO4] è collegata agli altri gruppi nel reticolo da solo tre ponti ad ossigeno e non quattro come ad esempio nella SiO2 (punto di Littleton 600°C). Come osserviamo dalla figura i vetri sodio-silicatici occupano una posizione intermedia tra i casi limite dei vetri di silice e di anidride borica.
1.3.2) Sistemi policomponenti
Fig.7
§ 5.9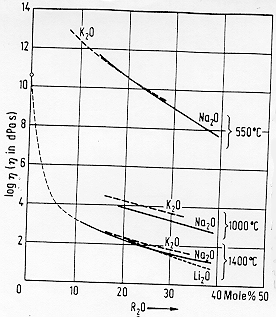
Nel grafico superiore della figura 7§ 5.9 viene mostrato come varia la viscosità in funzione della concentrazione molare di ossidi alcalini in un vetro di silice pura; all’aumentare della concentrazione l’aumento del numero di ossigeni non a ponte causa un indebolimento della struttura.
Ad alte temperature (sopra i 1000°C) e alte concentrazioni molari si nota che negli ioni con maggiore forza di campo c’è una tendenza maggiore alla coordinazione degli atomi di ossigeno: la superiore capacità polarizzante dello ione litio indebolisce il legame Si-O-Si più di quanto non faccia il potassio e questo provoca la maggiore diminuzione della viscosità osservata. In questo caso è evidente come l’influenza di un componente in un vetro sia legata alla sua percentuale molare ed alla temperatura.
Nel caso di miscele complesse come nel caso dell’aggiunta di un componente ad un sistema sodio-silicatico le cose sono più complicate, nei grafici in basso della figura 7 § 5.9 viene mostrata la relazione tra temperatura e percentuale molare a viscosità costante.
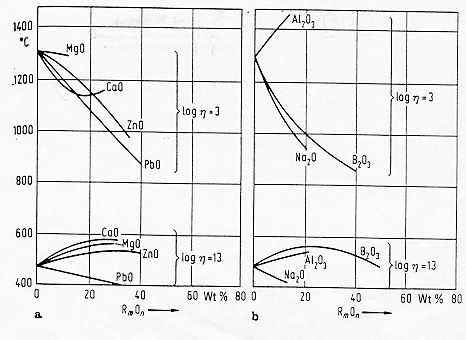
Per il calcio alle alte temperature (e bassi valori di viscosità) il comportamento è inizialmente simile a quello osservato in precedenza per gli elementi alcalini aggiunti ad un vetro di silice: l’aumento degli ossigeni non a ponte indebolisce la struttura e conseguentemente diminuisce la temperatura alla quale il vetro raggiunge il valore di 3 del logaritmo della viscosità, a bassa temperatura e comunque con alte percentuali molari di calcio aggiunto prevale la tendenza alla coordinazione degli ossigeni non a ponte formatisi: questi vengono allora eliminati nella struttura con un conseguente aumento della viscosità, in definitiva con l’introduzione di una percentuale di calcio variabile tra il 5 ed il 15 % molare si nota un contemporaneo abbassamento della viscosità alle alte temperature ed un innalzamento della medesima alle basse temperature, il vetro diventa più corto.
Questo fenomeno ha anche importanti ricadute nella tecnologia ceramica: le fritte da monocottura ad esempio contengono calcio e zinco (ossido che ha sotto questo profilo un comportamento analogo a quello del calcio) in questo modo l’intervallo tra la temperatura in cui la fritta è "ferma" e quella in cui la fritta è completamente fusa e distesa sul supporto è piuttosto basso: la fritta si conserva cioè allo stato solido fino ad una temperatura sufficientemente alta affinché la degasazione del supporto possa avvenire senza problemi attraverso la sua struttura ancora molto porosa e poi fonde con un piccolo delta di temperatura (vetro corto) assumendo un valore di viscosità sufficientemente basso da permettere la completa "stesura" della fritta nei brevi tempi imposti dalla tecnologia della monocottura rapida (35-45 minuti).
Anche per il MgO ed il BaO a bassa temperatura si fa sentire l’effetto della coordinazione e questo si riflette in pratica i un rafforzamento dei legami ed in un aumento della viscosità, tuttavia ad alta temperatura il Magnesio ha un andamento divergente rispetto al calcio: in questo caso esso tende ad assumere una coordinazione 4 e quindi una propensione al "network forming", l’effetto complessivo è quello che la viscosità non sembra influenzata dalla composizione. Per questa ragione i sistemi vetrosi in cui sono presenti calcio e magnesio mostrano una scarsa prevedibilità teorica con minimi pronunciati e non linearità.
L’introduzione del piombo come PbO come anche gli ossidi degli elementi della transizione ha come effetto quello di abbassare la viscosità alle alte come alle basse temperature: questo fenomeno è dovuto alla forte polarizzabilità dello ione Pb++, per lo zinco l’effetto della sua polarizzabilità si fa sentire soprattutto alle alte temperature mentre per basse temperature prevale la sua relativamente alta forza di campo con una più spiccata capacità di coordinare ossigeni; come comportamento complessivo quindi lo zinco si comporta come il calcio.
L’introduzione del Al2O3 porta come conseguenza l’eliminazione di ossigeni non a ponte, infatti in un sistema sodio-silicatico fintanto che il rapporto molare tra Na e Al è maggiore di uno il gruppo [AlO4]- tende a complessare il metallo alcalino network modifier: la viscosità aumenta sia a bassa che ad alta temperatura con l’aumentare della percentuale molare di allumina, tuttavia non appena il rapporto molare Na/Al diventa minore dell’unità non ci sono più cationi da complessare e l’alluminio perde la coordinazione 4 per passare alla coordinazione 6 tornando a svolgere la funzione di network modifier, per questa ragione aggiunte anche minime di allumina possono far drasticamente abbassare la viscosità di un vetro. Questo fenomeno è stato anche osservato negli smalti: è comune che piccole aggiunte di allumina alla formulazione di uno smalto a base di allumino, silice e ossidi alcalini ed alcalino-terrosi renda lo smalto stendibile contrariamente al senso comune.
L’effetto dell’introduzione del B2O3 nei vetri alcalino-silicatici § 5.9 è quello di far diminuire la viscosità a alta temperatura (log h =3) per la formazione progressiva di gruppi [BO3] ma di farla aumentare a temperatura più bassa (log h =3) per la formazione di gruppi [BO4]- "glass forming", l’effetto è quindi di rendere un vetro più corto o uno smalto adatto per la monocottura.
In sistemi alcalino-silicatici gli ioni Ti4+ e Zr4+ tendono nel reticolo a sostituire la silice, inoltre la loro forte tendenza alla coordinazione fa aumentare in maniera cospicua la viscosità dei sistemi vetrosi a cui sono aggiunti, per queste ragioni questi ossidi vengono anche denominati "refrattari".
Vetri alcalino-boratici, anomalia del boro
Fig. 8
§ 5.10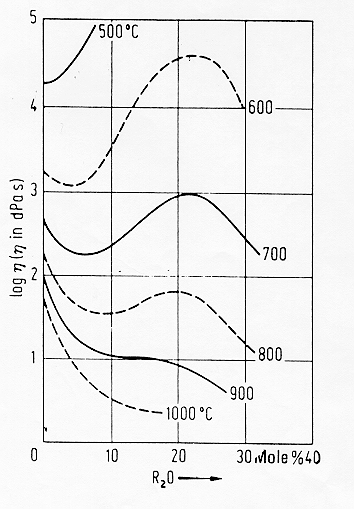
Per quanto riguarda i borati alcalini vediamo dalla figura 8 § 5.10 che all’aumentare della concentrazione di ossido R2O la viscosità aumenta in maniera evidente a temperature relativamente basse, questo è dovuto alla formazione dell’unità strutturale [BO4]- tetraedrica la cui valenza è saturata dallo ione alcalino tuttavia a tenori di alcali più elevati è l’effetto del catione "network modifier" a prevalere e la viscosità torna a diminuire. Ad alte temperature si somma un altro effetto: il boro, all’aumentare della temperatura tende a tornare alla sua usuale coordinazione 3 in una geometria trigonale tipo sp2 i gruppi planari [BO3] hanno la possibilità di legarsi solo attraverso 3 ponti ad ossigeno e la struttura si indebolisce: l’effetto complessivo è quello che osserviamo: una serie di curve con caratteristici massimi via via meno accentuati all’aumentare della temperatura, questo comportamento non lineare della viscosità con l’aumentare della concentrazione degli ossidi alcalini (ma è presente anche con altri tipi di ossidi) prende il nome di anomalia del boro.
Nella tecnologia del vetro e delle fritte da ceramica grande effetto hanno sulla viscosità del fuso la presenza nel batch di impurezze, in particolar modo di metalli di transizione, questi effetti si fanno soprattutto sentire a temperature relativamente basse, in genere quelle della formatura, o nel raffreddamento del rivestimento dei supporti ceramici creando problemi e difetti.
Ad esempio gli ioni OH- comportandosi come modificatori di reticolo fanno abbassare la viscosità del vetro: durante il processo di fusione il fuso è a contatto della atmosfera del forno che può contenere vapor d’acqua, in questo modo una certa percentuale di ioni OH- penetrano nel reticolo, è stato calcolato che la percentuale di acqua dissolta in un vetro fuso in atmosfera secca è dello 0,004% mentre sale allo 0,03% nel caso che lo stesso vetro sia stato fuso in una atmosfera satura di vapor d’acqua; questo si traduce in un abbassamento in quest’ultimo caso di un fattore 2 del logaritmo della viscosità. I forni elettrici producono vetri che contengono lo 0,01% di acqua dissolta contro lo 0,03% di acqua dissolta in vetri prodotti da forni a gas e questo ha una influenza sulla viscosità del fuso e in definitiva sulla sua lavorabilità.
1.4) Modelli matematici
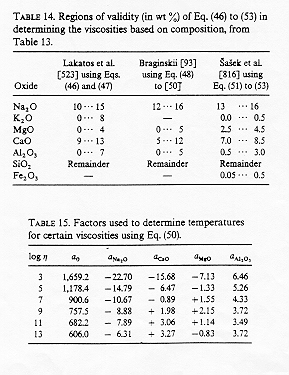
La viscosità come la maggior parte delle proprietà dei vetri è una proprietà additiva cioè varia in modo proporzionale con la percentuale (in genere molare) degli ossidi componenti. Come vediamo Lakatos propone un modello derivato dalla equazione V.F.T:
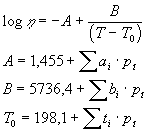
dove come vediamo pi è la frazione molare degli ossidi componenti il vetro e ai, bi e ti sono dei coefficienti moltiplicativi caratteristici di ciascun componente.
Braginskii propone un altro modello:
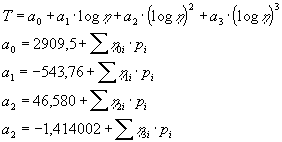
dove pi sono le frazioni in peso dei componenti ed h ji i fattori caratteristici per ciascun ossido.
Sasek ed Al. usa invece la formula:
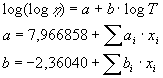
dove xi rappresentano trasformazioni di coordinate tali che se pi sono le frazioni % in peso si ha:
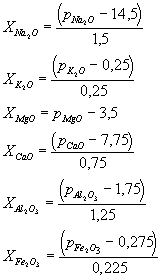
In figura 9 sono riportati i valori dei coefficienti per i vari modelli mentre in figura 10 :
Fig.9
§ 5.12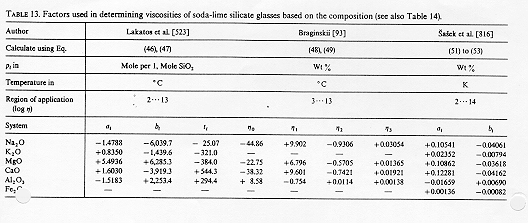
Fig.11
1.5) Implicazioni tecnologiche del diagramma della viscosità
Fig. 11
§ 5.13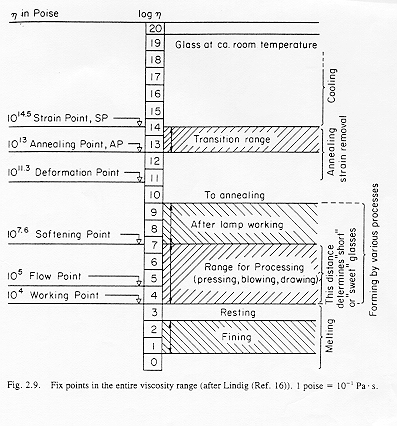
Nella figura 11 § 5.13 osserviamo la correlazione tra la viscosità e le problematiche tecnologiche legate alla lavorabilità del vetro: vediamo di definire meglio i punti caratteristici.
1.5.1) Temperatura di strain point h = 1014,5 Poise
è quella temperatura per la quale un vetro subisce il rilassamento delle tensioni indotte ad un valore del 10% del totale in 15 h. Costituisce il limite inferiore della zona di annealing in cui vengono rimossi gli stress termici per rilassamento.
1.5.2) Temperatura dell’annealing point h = 1013 Poise
è quella temperatura per la quale un vetro subisce il rilassamento delle tensioni indotte ad un valore del 10% del totale in 15 min. Costituisce il limite superiore della zona di annealing in cui vengono rimossi gli stress termici per rilassamento.
1.5.3) Temperatura del deformation point h = 1011,3 Poise
è anche la temperatura del rammollimento dilatometrico, costituisce il limite inferiore del range di formatura in particolari processi tecnologici del vetro.
1.5.4) Temperatura del softening point (o Littleton point) h = 107,6 Poise
e la temperatura alla quale un filamento di vetro di 23,5 cm di lunghezza e di diametro compreso tra 0,55 e 0,77 mm si allunga di 1mm/min, rappresenta il limite inferiore del range di processo di numerosi processi tecnologici ( formatura di bottiglie, vetri piani ...).
1.5.4) Temperatura del working point h = 104 Poise
in genere viene determinata per mezzo di un viscosimetro rotazionale, rappresenta il limite inferiore del range di processo.
In tabella 2 è riportato un quadro riassuntivo dei punti caratteristici con una loro breve descrizione.
Tab. 2 :
|
Valori di log h |
Definizione del punto caratteristico |
Descrizione |
|
log h = 2
log h = 3 |
"Melting Point"
"Gob Point" |
Corrisponde a temperature prossime a quelle di fusione Rappresenta la temperatura di goccia nella produzione dei contenitori ovvero l’inizio della formatura dei medesimi |
|
log h = 4
log h = 7.6 |
"Working Point"
"Littleton Point" |
Temperatura molto prossima all’inizio formatura del vetro piano, nonché alla temperatura di liquidus nei processi di devetrificazione Temperatura vicina a quella di fine formatura. |
|
log h = 13
log h = 14.5 |
"Annealing Point"
"Strain Point" |
Temperatura corrispondente a quella superiore di ricottura. E' quella temperatura alla quale un vetro subisce un rilassamento delle tensioni ad un valore pari al 10% del totale in 15 min. Temperatura che compete al punto inferiore di ricottura. E' quella temperatura alla quale un vetro subisce un rilassamento delle tensioni ad un valore pari al 10% del totale in 15 h. |